主诉
【病例摘要】
【病史】
患者男性,65岁,因上腹部不适1个月于2010年9月来我院胃肠外科就诊。
【现病史及家族史】
患者1个月前无明显诱因出现上腹部不适、胀痛,无反酸、嗳气,无腹泻及黑便。母亲有“胃癌”病史。入院时生命体征平稳,巩膜无黄染,左锁骨上淋巴结未及,腹平软,未及明显包块,无明显压痛、反跳痛,移动性浊音(-),肠鸣音正常,**指诊未及异常。
【入院检查】
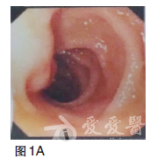
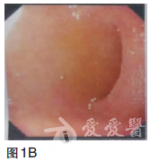
血常规无明显异常;血液生化检查未见明显异常;肿瘤标志物:癌胚抗原(CEA)69.28ng/ml.胃镜检查(2010年9月),提示贲门下胃体后壁见巨大溃疡,病变累及贲门口及胃底,大小约4×3cm,周边黏膜不规则(图1)。图1胃镜(2010年9月)贲门下胃体后壁见巨大溃疡,病变累及贲门口及胃底,大小约4×3cm,周边黏膜不规则病理检查为腺癌。CT检查(2010年9月),提示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影,考虑转移结节(图2)。
【病理检查】
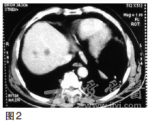
为腺癌。CT检查(2010年9月),提示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影,考虑转移结节(图2)png]图2CT(2010年9月)示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影
【MDT讨论及诊治经过】
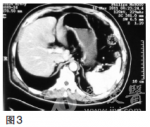
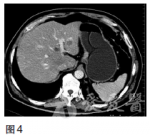
第一次MDT讨论(2010年10月)影像科该患者CT提示贲门下胃体小弯侧胃壁增厚,结合胃镜检查报告,胃癌诊断明确;CT示肝内多发低密度影,结合肿瘤标志物甲胎蛋白(AFP)不高,CEA考虑为转移结节,诊断为胃癌伴肝转移。肿瘤内科多数胃癌肝转移患者,全身化疗是主要治疗方法,但胃癌化疗目前尚无标准方案。常用化疗药5-氟尿嘧啶(5-Fu)及其前体药的口服剂(卡培他滨、替吉奥)、紫杉类(紫杉醇、多西他赛)、铂类(顺铂、奥沙利铂)。针对该患者可采用DCF3周方案。胃肠外科胃癌肝转移根据美国**综合癌症网络(NCCN)胃癌临床实践指南,主要采用化疗、纳入临床研究和最佳支持治疗等姑息措施。然而,也有一些研究表明对胃癌肝转移进行积极的综合治疗仍可使部分患者生存获益。治疗方案的选择应从以下方面考虑:①是同时性肝转移还是异时性肝转移;②评估肝脏转移灶大小、部位及多少,H1为转移灶局限于一个肝叶,H2为两个肝叶可见数个散在转移灶,H3为两个肝叶可见多量散在转移灶;③肝外有无转移灶;④原发病灶能否完全切除(R0)。对于原发灶能R0切除的H1型肝转移以及异时性肝转移应积极行一期联合切除或肝转移灶切除,而对于H2和H3型同时性肝转移,手术作为综合治疗手段之一可能有一定价值,但应慎重选择病例。肝脏外科对于胃癌肝转移的多个转移灶,建议行化疗、射频或介入等综合治疗,对孤立转移灶可考虑手术切除。针对该患者,建议化疗为主,手术为辅。消化内科对于中晚期胃癌,一般不考虑内镜下治疗。该患者无内镜下治疗的适应证。第一次治疗经过2010年10月采用DCF3周方案[多西他赛100mg/m2,第1天;顺铂20mg,1次/日,第1——5天;5-Fu750mg/m2,1次/日,第1——5天,每日持续静脉滴注6小时以上],解救化疗4个周期后,CT检查示胃壁肿块及肝转移灶均较前缩小,同前方案治疗共6个周期。2011年3月复查CEA48.26ng/ml,CT检查(图3)示贲门部胃壁增厚不明显,肝内未见明确低密度结节,复查胃镜示贲门下胃体后壁黏膜不规则隆起,2×2cm,累及贲门,临床评价部分缓解,改卡培他滨单药维持。图3CT(2011年3月)示贲门部胃壁增厚不明显,肝内未见明确低密度结节2011年9月CEA升高为91.20ng/ml,CT示肝脏转移灶增大(图4)。图4CT(2011年9月)示肝脏转移灶再次出现2011年9月再次组织全院胃癌MDT讨论。
【第二次MDT】
讨论(2011年9月)影像科2011年9月CT检查示贲门部胃壁增厚,肝脏内见数个圆形低密度影,大小分别为2.8×2.4cm、1.2×1.1cm、1.1×1.0cm,与周围组织分界欠清,结合第一次的CT,考虑肝多发转移,胃癌复发。肿瘤内科患者目前胃癌复发,在DCF方案效果不佳情况下,可考虑TCF(紫杉醇+顺铂+替加氟)等方案,也可考虑其他化疗方案,患者耐受性很差的情况下甚至可选择卡培他滨或替吉奥单药化疗。针对该患者建议行人表皮生长因子受体2(HER2)等相关检测,以决定是否需要考虑联合靶向药物治疗。胃肠外科胃癌肝转移手术治疗是一种姑息性治疗手段,在没有并发症前提下手术意义不大。针对该患者用改良DCF方案化疗6个周期,卡培他滨单药维持后,转移灶消失后复现,无梗阻、出血等并发症,无法R0切除,不建议手术。肝脏外科患者目前仍不具备肝脏转移灶R0切除条件,仍不建议手术。介入科该患者属于胃癌合并同时性肝脏多灶性转移,通过一线化疗方案,肝脏转移灶消失后复现,CEA升高。由于胃病灶与肝脏转移灶均存在,介入治疗无法完全根治。目前可参考肿瘤科的意见,更换二线化疗方案,当二线方案失效后,再考虑介入治疗。
【第二次治疗经过】
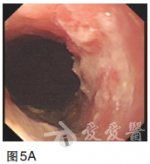
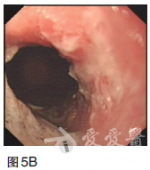
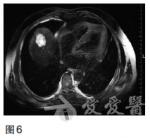
2011年9月采用TOF二线方案化疗(紫杉醇60mg/m2,第1、8天;奥沙利铂65mg/m2,第1、8天;5-Fu750mg/m2,1次/日,第1——5天,每日持续静脉滴注6小时以上,3周为一疗程,两个疗程后复查CT提示肝多发转移灶较前缩小,原最大病灶变为1.7×1.5cm.2012年1月继续维持此方案化疗4个周期后,患者耐受良好,改卡培他滨单药口服维持。2013年4月定期复查CT和CEA等肿瘤标志物,病情时有反复,交替更换化疗方案对症处理至今,目前一般状况尚可,时有上腹不适及乏力等症状,胃镜检查示贲门下胃体后壁见黏膜高低不平,大小约4×4cm(图5)。图5胃镜检查(2013年4月)示贲门下胃体后壁见黏膜高低不平,大小约4×4cm磁共振成像(MRI)检查示肝内多发转移结节较前增多增大(图6),CEA170.48ng/ml,行进一步治疗中。图6MRI(2013年4月)示肝内多发转移结节较前增多增大
【MDT治疗体会】
肝脏是胃癌远处转移最常见的靶器官。术前已明确或术中发现的肝转移占2.0%——9.9%.胃癌肝转移(GCLM)不仅预后差(5年生存率
查体
【病例摘要】
【病史】
患者男性,65岁,因上腹部不适1个月于2010年9月来我院胃肠外科就诊。
【现病史及家族史】
患者1个月前无明显诱因出现上腹部不适、胀痛,无反酸、嗳气,无腹泻及黑便。母亲有“胃癌”病史。入院时生命体征平稳,巩膜无黄染,左锁骨上淋巴结未及,腹平软,未及明显包块,无明显压痛、反跳痛,移动性浊音(-),肠鸣音正常,**指诊未及异常。
【入院检查】
血常规无明显异常;血液生化检查未见明显异常;肿瘤标志物:癌胚抗原(CEA)69.28ng/ml.胃镜检查(2010年9月),提示贲门下胃体后壁见巨大溃疡,病变累及贲门口及胃底,大小约4×3cm,周边黏膜不规则(图1)。图1胃镜(2010年9月)贲门下胃体后壁见巨大溃疡,病变累及贲门口及胃底,大小约4×3cm,周边黏膜不规则病理检查为腺癌。CT检查(2010年9月),提示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影,考虑转移结节(图2)。



【病理检查】
为腺癌。CT检查(2010年9月),提示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影,考虑转移结节(图2)png]图2CT(2010年9月)示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影
【MDT讨论及诊治经过】
第一次MDT讨论(2010年10月)影像科该患者CT提示贲门下胃体小弯侧胃壁增厚,结合胃镜检查报告,胃癌诊断明确;CT示肝内多发低密度影,结合肿瘤标志物甲胎蛋白(AFP)不高,CEA考虑为转移结节,诊断为胃癌伴肝转移。肿瘤内科多数胃癌肝转移患者,全身化疗是主要治疗方法,但胃癌化疗目前尚无标准方案。常用化疗药5-氟尿嘧啶(5-Fu)及其前体药的口服剂(卡培他滨、替吉奥)、紫杉类(紫杉醇、多西他赛)、铂类(顺铂、奥沙利铂)。针对该患者可采用DCF3周方案。胃肠外科胃癌肝转移根据美国**综合癌症网络(NCCN)胃癌临床实践指南,主要采用化疗、纳入临床研究和最佳支持治疗等姑息措施。然而,也有一些研究表明对胃癌肝转移进行积极的综合治疗仍可使部分患者生存获益。治疗方案的选择应从以下方面考虑:①是同时性肝转移还是异时性肝转移;②评估肝脏转移灶大小、部位及多少,H1为转移灶局限于一个肝叶,H2为两个肝叶可见数个散在转移灶,H3为两个肝叶可见多量散在转移灶;③肝外有无转移灶;④原发病灶能否完全切除(R0)。对于原发灶能R0切除的H1型肝转移以及异时性肝转移应积极行一期联合切除或肝转移灶切除,而对于H2和H3型同时性肝转移,手术作为综合治疗手段之一可能有一定价值,但应慎重选择病例。肝脏外科对于胃癌肝转移的多个转移灶,建议行化疗、射频或介入等综合治疗,对孤立转移灶可考虑手术切除。针对该患者,建议化疗为主,手术为辅。消化内科对于中晚期胃癌,一般不考虑内镜下治疗。该患者无内镜下治疗的适应证。第一次治疗经过2010年10月采用DCF3周方案[多西他赛100mg/m2,第1天;顺铂20mg,1次/日,第1——5天;5-Fu750mg/m2,1次/日,第1——5天,每日持续静脉滴注6小时以上],解救化疗4个周期后,CT检查示胃壁肿块及肝转移灶均较前缩小,同前方案治疗共6个周期。2011年3月复查CEA48.26ng/ml,CT检查(图3)示贲门部胃壁增厚不明显,肝内未见明确低密度结节,复查胃镜示贲门下胃体后壁黏膜不规则隆起,2×2cm,累及贲门,临床评价部分缓解,改卡培他滨单药维持。图3CT(2011年3月)示贲门部胃壁增厚不明显,肝内未见明确低密度结节2011年9月CEA升高为91.20ng/ml,CT示肝脏转移灶增大(图4)。图4CT(2011年9月)示肝脏转移灶再次出现2011年9月再次组织全院胃癌MDT讨论。


【第二次MDT】
讨论(2011年9月)影像科2011年9月CT检查示贲门部胃壁增厚,肝脏内见数个圆形低密度影,大小分别为2.8×2.4cm、1.2×1.1cm、1.1×1.0cm,与周围组织分界欠清,结合第一次的CT,考虑肝多发转移,胃癌复发。肿瘤内科患者目前胃癌复发,在DCF方案效果不佳情况下,可考虑TCF(紫杉醇+顺铂+替加氟)等方案,也可考虑其他化疗方案,患者耐受性很差的情况下甚至可选择卡培他滨或替吉奥单药化疗。针对该患者建议行人表皮生长因子受体2(HER2)等相关检测,以决定是否需要考虑联合靶向药物治疗。胃肠外科胃癌肝转移手术治疗是一种姑息性治疗手段,在没有并发症前提下手术意义不大。针对该患者用改良DCF方案化疗6个周期,卡培他滨单药维持后,转移灶消失后复现,无梗阻、出血等并发症,无法R0切除,不建议手术。肝脏外科患者目前仍不具备肝脏转移灶R0切除条件,仍不建议手术。介入科该患者属于胃癌合并同时性肝脏多灶性转移,通过一线化疗方案,肝脏转移灶消失后复现,CEA升高。由于胃病灶与肝脏转移灶均存在,介入治疗无法完全根治。目前可参考肿瘤科的意见,更换二线化疗方案,当二线方案失效后,再考虑介入治疗。
【第二次治疗经过】
2011年9月采用TOF二线方案化疗(紫杉醇60mg/m2,第1、8天;奥沙利铂65mg/m2,第1、8天;5-Fu750mg/m2,1次/日,第1——5天,每日持续静脉滴注6小时以上,3周为一疗程,两个疗程后复查CT提示肝多发转移灶较前缩小,原最大病灶变为1.7×1.5cm.2012年1月继续维持此方案化疗4个周期后,患者耐受良好,改卡培他滨单药口服维持。2013年4月定期复查CT和CEA等肿瘤标志物,病情时有反复,交替更换化疗方案对症处理至今,目前一般状况尚可,时有上腹不适及乏力等症状,胃镜检查示贲门下胃体后壁见黏膜高低不平,大小约4×4cm(图5)。图5胃镜检查(2013年4月)示贲门下胃体后壁见黏膜高低不平,大小约4×4cm磁共振成像(MRI)检查示肝内多发转移结节较前增多增大(图6),CEA170.48ng/ml,行进一步治疗中。图6MRI(2013年4月)示肝内多发转移结节较前增多增大



【MDT治疗体会】
肝脏是胃癌远处转移最常见的靶器官。术前已明确或术中发现的肝转移占2.0%——9.9%.胃癌肝转移(GCLM)不仅预后差(5年生存率
























全部评论
该病人加重原因:1、不规范治疗:饮酒、生气,就诊晚 2、脑梗死本身就是一个病情变化的过程,有的加重,有的逐渐减轻,这取决于很多因素:梗死的面积、部位、救治时间、脑细胞代偿功能、侧枝循环的情况3、病情加重谁都不愿意见到,要向家属做好解释说服工作
楼主分析的很好,再把用药还有后续治疗情况传上就更好了
该病人加重原因:1、不规范治疗:饮酒、生气,就诊晚 2、脑梗死本身就是一个病情变化的过程,有的加重,有的逐渐减轻,这取决于很多因素:梗死的面积、部位、救治时间、脑细胞代偿功能、侧枝循环的情况3、病情加重谁都不愿意见到,要向家属做好解释说服工作
其实这样的病例临床很普遍,由该病例,请各位爱友继续探讨下下面问题: 1 中药制剂,现在临床应用非常多,如银杏注射液,血栓通,各类含有红花、水蛭等“活血”类胶囊,这些药早期运用,有没有循征依据,是否会加重脑梗死症状? 2 一些腔隙性脑梗死病人病情进行性加重,机理是什么?怎么防止症状加重?早期干预如何做到有效?
我考虑第一次行颅脑CT有梗塞灶,不知是否是责任梗塞灶,第二次已经发病12天了,接近颅脑CT的模糊效应期,但这个病灶对比第一次的CT应该是新鲜的,是瘫痪的原因,可以行颅脑MRI检查,看两次病灶的密度值有无一致。治疗应该抗血小板、抗凝、活血化瘀及稳定血压、血脂积极治疗,根据家庭情况看能否用起必存,效果应该不错的。 和应用药物、饮酒都无关,就是耽误治疗,错过时机了。
梗死扩大原因: 1. 外在因素:饮酒、非正规治疗 2.内在因素:局部血管初期为狭窄,逐渐为闭塞。其发展过程是诸多因素参与的病生理变化。 治疗 1.吸氧 2.调控血压:维持在基础血压或稍高水平。 3.扩容:降低血液黏稠性,还可增加血容量维持血压 4.抗凝:阿司匹林、氯比格雷、低分子肝素等。 5.改善脑代谢药物 6.合并症、并发症及其他脏器病变的预防和治疗,营养支持。 7.瘫痪肢体的功能位及被动运动 具体治疗应根据病人的具体情况个体化治疗。
1患者为什么会梗死灶增大?与用多种活血化瘀药有关还是与饮酒有关? 静脉推注小牛血去蛋白提取物注射液: 可增强组织细胞对氧及葡萄糖摄取与利用作用,改善细胞乏氧状态和机体内环境,增加心、脑、肝等脏器的血流量,改善微循环。 脉血康: 实验证明,本品能有效抑制血栓形成和血小板粘附,明显缩短红细胞电泳时间,降低血清胆固醇TC及血清甘油三酯TG,较强的延长血浆复钙,凝血酶原时间,改善微循环,具强的纤溶活性和抗凝血活性。 这里有一个比较明显的问题,那就是对于急性脑血管疾病发作的病人首先应测量血压,然后应补充血糖检查以及进行凝血功能检查。 对于该患者,还应该进行脑血管造影,这样才能了解血栓和栓子的准确位置。 在缺血性卒中最初发生的48小时之内除了阿司匹林之外的其它抗凝药物是不推荐使用的,因为它们都有可能造成缺血性损伤的进一步加重。对急性患者进行一般支持疗法时也应当注意,过多的液体进入神经元可使缺血性损伤进一步加重。 理论上降低血压可减少患者梗死后出血危险性,防止脑血管进一步损害,并预防脑血管进一步损害。但血压低会降低脑灌注压。脑卒中后脑血流自动调节功能受损,缺血半暗带的脑血流量与平均动脉压呈正相关,血压升高是脑卒中机体的一种代偿反应,目的要维持脑灌注压。若血压下降过快将使脑部供血减少,使得缺血或梗死的范围扩大,反之,特别是使用了溶栓药物治疗以后,高血压又会使脑出血的发病危险增加。因此,高血压病人的处理,不仅要维持适度的脑灌注压,还要防止高血压对患者的损害。 高血糖能加重脑组织的损害,加重缺血脑组织的神经元坏死,扩大梗死灶范围,使病死率增加。因此也应注意病人的血糖标准。 由于腔隙性脑梗死病灶小,一般不引起占位效应,脱水降颅内压无效,故若无明显颅内高压症,应避免使用脱水、利尿剂,以防血液进一步浓缩,使脑梗死症状加重。 脑缺血发生后,半暗带区神经元面临两种结局,一种是局部微环境改善情况下,功能受损的神经元重新恢复,另外一种是局部微环境持续恶化而诱发神经元凋亡,是梗死灶扩大和迟发性神经元损伤的主要机制。 上述的每一步错误都有可能导致患者的梗死面积扩大,使得病情加重。个人认为,使用的药物并不足以导致梗死面积的改变,所以应该与患者饮酒有很大关系。 2下一步如何治疗? 血压若无明显升高,一般不宜降压,但是当收缩压高于220 mmHg、舒张压高于120 mmHg 或平均动脉压高于130 mmHg 时必须要采取降压,应及时应用降压药将血压逐渐降至卒中前水平或150~160 mmHg/90~100 mmHg 左右。 增加脑血流量,改善脑微循环。 使用脑细胞活化药通过阻断由缺血所致各种有害病理过程的发生,从而防止由局部缺血所引起的脑损害,减少脑细胞死亡和促进功能恢复。 加强支持治疗以及并发症的处理。