小儿胰母细胞瘤3例
发布人:

g****g其他医务者
更新时间:2018-05-11 10:32
关注
【病案介绍】
主诉
病例1,女,2岁
病例2,男,4岁
病例3,女,8岁
病例1,因发现腹部肿物1 d入院。
病例2,因阵发性腹痛伴呕吐3年余,发现左上腹肿块2 d入院
病例3 因腹胀、纳差伴面色苍白1月余入院。
查体
病例1,全腹膨隆,以左中上腹明显,左侧腹可扪及一巨大包块,肝脾肋下未触及。
病例2,左上腹稍隆起,可触及一质硬包块,肝脾肋下未触及。
病例3,全身皮肤苍白,结膜苍白。腹部膨隆,可触及一质硬包块,肝脾肋下未触及。
辅助检查
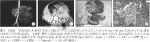
病例1,血液检查提示:WBC 9.5x109/L,HGB 97 g/L,PLT 567x109/L,肝功能正常。肿瘤标志物检查提示:AFP、NSE、CYFRA21-1值升高,CA125、CEA均正常。腹部彩超提示:左肾中下部内侧见一约7.4 cm×6.4 cm×8.2 cm大小的实性低回声包块,与左肾及胰尾分界不清,内回声欠均匀,可见密集点状强回声及散在不规则无回声区。腹部CT检查提示:左侧腹膜后可见类圆形软组织密度影,其内密度不均,增强扫描呈不均匀明显强化(图A、图B)。
病例2,血生化检查提示:WBC 13.2x109/L,HGB 120 g/L,PLT 938×109/L,肝功能正常。肿瘤标志物提示:AFP、CYFRA211值升高,CA125、NSE、CEA均在正常范围。
腹部彩超提示:左肾上腺区可见16.1 cmx8.3 cmx10.2 cm实性低回声,其后方紧邻胰尾,边界尚清,其内回声强弱不均,并可见密集点状强回声,内可见丰富血流信号。腹部CT检查提示:左肾前上方可见一巨大团块状软组织影,其内密度不均,并可见斑片状低密度影及点条状高密度影,周围肠管、胰腺及左肾受压移位,增强病灶呈不均强化。
病例3,血生化检查提示:WBC 12.7×109/L,HGB 48 g/L,PLT 355X109/L,肝功能均正常,肿瘤标志物提示:CA125、NSE值升高,CEA、AFP、CYFRA211均正常,腹部彩超提示腹腔内可见不均质回声团,约25 cm x18 cm x20 cm,上界位于剑突下,下界平脐,边界不清,内可见不规则液性暗区。
CT检查可见肝脾间、脾脏弥漫性巨大占位,密度不均匀,边界不清。增强后呈不均匀强化,其内可见动脉血管影,肝脏呈受压改变,实质内未见异常密度及强化影,胰腺显示不清。
【诊治过程】
初步诊断
病例1,腹腔巨大占位性病变:神经母细胞瘤待查?
病例2,左上腹占位性病变:神经母细胞瘤?畸胎瘤?
病例3,腹腔内巨大占位:神经母细胞瘤?
诊治经过
病例1,术中探查见肿块位于左侧腹膜后脾肾之间,直径约8 cm,胰腺体尾部紧贴瘤体,并有较多血管相连,脾静脉血管紧贴瘤体(图C),因粘连紧密无法分离。术中行肿瘤+胰体尾+脾脏切除术。
病理检查结果提示:恶性肿瘤,考虑胰腺来源,倾向胰母细胞瘤。免疫组化结果:Syn(部分+),CgA(-),CEA(-),CK(+),AFP(灶+),AAT(+),CD99(+),CD56(-),Vimentin(-),Ki - 67(40%)(图D),结合病理检查结果诊断为胰母细胞瘤。术后分别予THP +CDDP(吡柔比星、顺铂)、VP-16+ CDDP(依托泊苷、顺铂)方案化疗,并结合DC-CIK方案予生物治疗,术后7个月,复查腹部CT,未见肿瘤转移及复发,AFP正常。
病例2,术中探查见肿瘤位于腹膜后偏左侧,似来源于胰腺体尾部,包膜不完整,大小约20 cmx12 cmx13 cm,形状似葫芦状,质硬实性,活动度差,上界至胃壁后方左侧膈肌下,下方至左侧肾下缘处。
术中行肿瘤+胰体尾切除术。病理检查结果提示:恶性肿瘤,考虑胰母细胞瘤。免疫组化提示:CK(+),Syn(+),Ki-67( 30~40%+),CEA(-),AAT(+),CD99(+) ,Vimentin(-),CgA(-),结合病理检查诊断为胰母细胞瘤。术后切口愈合良好,未及时行化疗,术后1年复查腹部CT,见肝内低密度影,约9.3 cmx6 cm大小,考虑转移。未再予手术治疗,分别给予THP +CDDP、VP-16+ CDDP方案化疗,并结合DC-CIK方案生物治疗,6个月后复查腹部CT,肝内肿块较前明显缩小,复查AFP正常。
病例3,术中见肿瘤位于左侧腹部,外有包膜,大小约30 cm×25 cm×18 cm,形状不规则,囊实性,可见多处囊内出血,无明显活动度,横跨脊柱两侧,上界侵及膈肌,将脾脏推至左上腹,压迫脾门,右界达胰腺中部,胰尾与瘤体无明显界限。下界达十二指肠水平部,后方紧邻腹主动脉,下腔静脉受挤压增宽。术中行肿瘤+胰体尾切除术。病理检查提示:小细胞恶性肿瘤,考虑胰母细胞瘤。免疫组化提示:CK(+),Syn(灶+),Ki-67( 40%+),CEA(-),AAT(+) ,CD99(+),Vimentin(-),CgA(-),结合病理检查诊断为胰母细胞瘤。患儿切口愈合良好,术后给予VCR+ CDDP+CTX(长春新碱、顺铂、环磷酰胺)、THP+ CDDP+CTX(吡柔比星、顺铂、环磷酰胺)方案化疗,术后14个月患儿因肿瘤复发并脑转移而死亡。
【其他】
【讨论】
胰母细胞瘤( Pancreatoblastoma,PB)是一种极罕见的胰腺恶性肿瘤,发病率约占儿童胰腺上皮样肿瘤的0. 5%。多见于婴幼儿,又称婴幼儿胰腺癌,1932年由Stout首先报道该病,以后多为个案报告。Horie等认为胰母细胞瘤来源于胰始基细胞,组织学特点与胚胎期胰腺相似,光镜下为胰腺器官样结构,中心为巢样结构或鳞状小体,环以髓样中间带,外围为腺泡样结构,与肾母细胞瘤、肝母细胞瘤、神经母细胞瘤类似,故提出胰母细胞瘤之名。
小儿PB无特异性临床表现,一般表现包括腹部包块、体重减轻、食欲不振、呕吐、腹痛、贫血等,本组3例均表现为腹部包块,1例表现为食欲不振,1例有腹痛伴呕吐,1例因肿瘤合并囊内出血表现为贫血。也有作者报道患者无任何临床部包块,1例表现为食欲不振,1例有腹痛伴呕吐,1例因肿瘤合并囊内出血表现为贫血。也有作者报道患者无任何临床X母细胞瘤,术后病理检查结果提示为PB。PB可有恶性肿瘤的临床特征,表现为浸润、转移和复发等。
彩超、CT、MRI均有辅助诊断意义。细致的产前检查有助于早发现、早诊断及早治疗。彩超检查可见异质性或低回声团块,有时可见少量液性暗区,肿瘤血管主要来源于肠系膜和下腔静脉,钙化不常见。在CT及MRI上肿瘤呈低密度灶,多房腔,并见增强的腔隔是PB的一大特点。ERCP常见主胰管阻塞,但胆管扩张不多见,因其检查困难,临床极少采用。
同时,在血清和免疫组织检测中有68%的PB患儿出现AFP升高。因此,AFP可作为PB -个重要的肿瘤标志物,有助于诊断和手术及化疗、生物治疗期间的随访。本组3例有2例术前AFP明显升高,术后随访恢复正常。
由于小儿胰母细胞瘤为胰腺恶性肿瘤,若能及时发现并手术彻底切除同时辅以化疗和放疗可延长生存期。有文献报道,PB以胰头部肿瘤为主,2/3的肿瘤发生在胰头,且多发生在胰头腹侧。81。本组3例瘤体均发生于胰腺体尾部,回顾其他相关病例报道,胰母细胞瘤发生于胰腺体尾部并不少见。手术要根据肿瘤部位、大小及与周围组织的关系、有无远处转移而定,常用手术为肿瘤局部切除和胰体尾切除术等。本组3例肿瘤均发生在胰腺体尾部,术中胰腺体尾部连同瘤体一并切除。术后予积极营养支持,防止水、电解质紊乱。
PB的治疗应首选手术治疗,文献报道多为肿瘤局部切除。祝秀丹认为扩大切除术( Whipple)手术难度大,并发症多,应慎重选择。而作为综合治疗的一部分,术前化疗可使肿瘤缩小,提高手术切除率,对于肿瘤已切除的患者,化疗能起到良好的辅助治疗效果。Ohata等报道1例胰头部胰母细胞瘤经化疗后肿瘤缩小,成功完成胰十二指肠根治手术,因而推荐胰头部胰母细胞瘤先化疗后手术。目前公认化疗有效,作者采用上海儿童医学中心胰母细胞瘤化疗方案,主要为THP+CDDP、VP-16+CDDP等。同时,放疗对PB也有效,此外,生物治疗作为一种新兴的肿瘤治疗模式,通过干扰肿瘤细胞的发生、生长、分化、凋亡、侵袭、转移和复发,促进机体免疫细胞重建,使细胞毒性物质集中于肿瘤组织,达到直接恢复和提高人体免疫功能,增强对肿瘤细胞的免疫力而实现肿瘤特异性治疗,主要包括细胞因子治疗、单克隆抗体治疗、过继性免疫细胞治疗、基因治疗、肿瘤疫苗治疗等,是目前肿瘤治疗的第4种方法。本组2例均采用DC-CIK方案生物治疗,属过继性免疫细胞治疗的一种,随访2例患儿预后良好。
病例来源:爱爱医
版权声明:站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,如果您认为我们的转载侵犯了您的权益,请及时通过电话(400-626-9910)或邮箱(zlzs@120.net)通知我们,我们将第一时间处理,感谢。

全部评论