【病案介绍】
主诉
【病例摘要】
【病史】
患者男性,65岁,因上腹部不适1个月于2010年9月来我院胃肠外科就诊。
【现病史及家族史】
患者1个月前无明显诱因出现上腹部不适、胀痛,无反酸、嗳气,无腹泻及黑便。母亲有“胃癌”病史。入院时生命体征平稳,巩膜无黄染,左锁骨上淋巴结未及,腹平软,未及明显包块,无明显压痛、反跳痛,移动性浊音(-),肠鸣音正常,**指诊未及异常。
【入院检查】
血常规无明显异常;血液生化检查未见明显异常;肿瘤标志物:癌胚抗原(CEA)69.28ng/ml.胃镜检查(2010年9月),提示贲门下胃体后壁见巨大溃疡,病变累及贲门口及胃底,大小约4×3cm,周边黏膜不规则(图1)。图1胃镜(2010年9月)贲门下胃体后壁见巨大溃疡,病变累及贲门口及胃底,大小约4×3cm,周边黏膜不规则病理检查为腺癌。CT检查(2010年9月),提示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影,考虑转移结节(图2)。
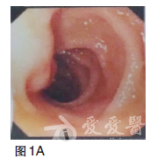
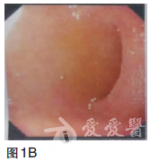
【病理检查】
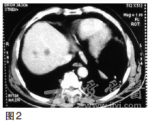
为腺癌。CT检查(2010年9月),提示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影,考虑转移结节(图2)png]图2CT(2010年9月)示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影
【MDT讨论及诊治经过】
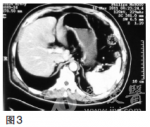
第一次MDT讨论(2010年10月)影像科该患者CT提示贲门下胃体小弯侧胃壁增厚,结合胃镜检查报告,胃癌诊断明确;CT示肝内多发低密度影,结合肿瘤标志物甲胎蛋白(AFP)不高,CEA考虑为转移结节,诊断为胃癌伴肝转移。肿瘤内科多数胃癌肝转移患者,全身化疗是主要治疗方法,但胃癌化疗目前尚无标准方案。常用化疗药5-氟尿嘧啶(5-Fu)及其前体药的口服剂(卡培他滨、替吉奥)、紫杉类(紫杉醇、多西他赛)、铂类(顺铂、奥沙利铂)。针对该患者可采用DCF3周方案。胃肠外科胃癌肝转移根据美国**综合癌症网络(NCCN)胃癌临床实践指南,主要采用化疗、纳入临床研究和最佳支持治疗等姑息措施。然而,也有一些研究表明对胃癌肝转移进行积极的综合治疗仍可使部分患者生存获益。治疗方案的选择应从以下方面考虑:①是同时性肝转移还是异时性肝转移;②评估肝脏转移灶大小、部位及多少,H1为转移灶局限于一个肝叶,H2为两个肝叶可见数个散在转移灶,H3为两个肝叶可见多量散在转移灶;③肝外有无转移灶;④原发病灶能否完全切除(R0)。对于原发灶能R0切除的H1型肝转移以及异时性肝转移应积极行一期联合切除或肝转移灶切除,而对于H2和H3型同时性肝转移,手术作为综合治疗手段之一可能有一定价值,但应慎重选择病例。肝脏外科对于胃癌肝转移的多个转移灶,建议行化疗、射频或介入等综合治疗,对孤立转移灶可考虑手术切除。针对该患者,建议化疗为主,手术为辅。消化内科对于中晚期胃癌,一般不考虑内镜下治疗。该患者无内镜下治疗的适应证。第一次治疗经过2010年10月采用DCF3周方案[多西他赛100mg/m2,第1天;顺铂20mg,1次/日,第1——5天;5-Fu750mg/m2,1次/日,第1——5天,每日持续静脉滴注6小时以上],解救化疗4个周期后,CT检查示胃壁肿块及肝转移灶均较前缩小,同前方案治疗共6个周期。2011年3月复查CEA48.26ng/ml,CT检查(图3)示贲门部胃壁增厚不明显,肝内未见明确低密度结节,复查胃镜示贲门下胃体后壁黏膜不规则隆起,2×2cm,累及贲门,临床评价部分缓解,改卡培他滨单药维持。图3CT(2011年3月)示贲门部胃壁增厚不明显,肝内未见明确低密度结节2011年9月CEA升高为91.20ng/ml,CT示肝脏转移灶增大(图4)。图4CT(2011年9月)示肝脏转移灶再次出现2011年9月再次组织全院胃癌MDT讨论。
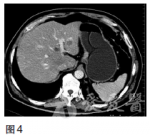
【第二次MDT】
讨论(2011年9月)影像科2011年9月CT检查示贲门部胃壁增厚,肝脏内见数个圆形低密度影,大小分别为2.8×2.4cm、1.2×1.1cm、1.1×1.0cm,与周围组织分界欠清,结合第一次的CT,考虑肝多发转移,胃癌复发。肿瘤内科患者目前胃癌复发,在DCF方案效果不佳情况下,可考虑TCF(紫杉醇+顺铂+替加氟)等方案,也可考虑其他化疗方案,患者耐受性很差的情况下甚至可选择卡培他滨或替吉奥单药化疗。针对该患者建议行人表皮生长因子受体2(HER2)等相关检测,以决定是否需要考虑联合靶向药物治疗。胃肠外科胃癌肝转移手术治疗是一种姑息性治疗手段,在没有并发症前提下手术意义不大。针对该患者用改良DCF方案化疗6个周期,卡培他滨单药维持后,转移灶消失后复现,无梗阻、出血等并发症,无法R0切除,不建议手术。肝脏外科患者目前仍不具备肝脏转移灶R0切除条件,仍不建议手术。介入科该患者属于胃癌合并同时性肝脏多灶性转移,通过一线化疗方案,肝脏转移灶消失后复现,CEA升高。由于胃病灶与肝脏转移灶均存在,介入治疗无法完全根治。目前可参考肿瘤科的意见,更换二线化疗方案,当二线方案失效后,再考虑介入治疗。
【第二次治疗经过】
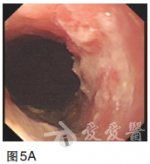
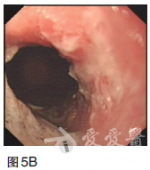
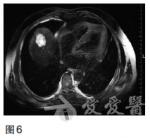
2011年9月采用TOF二线方案化疗(紫杉醇60mg/m2,第1、8天;奥沙利铂65mg/m2,第1、8天;5-Fu750mg/m2,1次/日,第1——5天,每日持续静脉滴注6小时以上,3周为一疗程,两个疗程后复查CT提示肝多发转移灶较前缩小,原最大病灶变为1.7×1.5cm.2012年1月继续维持此方案化疗4个周期后,患者耐受良好,改卡培他滨单药口服维持。2013年4月定期复查CT和CEA等肿瘤标志物,病情时有反复,交替更换化疗方案对症处理至今,目前一般状况尚可,时有上腹不适及乏力等症状,胃镜检查示贲门下胃体后壁见黏膜高低不平,大小约4×4cm(图5)。图5胃镜检查(2013年4月)示贲门下胃体后壁见黏膜高低不平,大小约4×4cm磁共振成像(MRI)检查示肝内多发转移结节较前增多增大(图6),CEA170.48ng/ml,行进一步治疗中。图6MRI(2013年4月)示肝内多发转移结节较前增多增大
【MDT治疗体会】
肝脏是胃癌远处转移最常见的靶器官。术前已明确或术中发现的肝转移占2.0%——9.9%.胃癌肝转移(GCLM)不仅预后差(5年生存率
现病史
【病例摘要】
【病史】
患者男性,65岁,因上腹部不适1个月于2010年9月来我院胃肠外科就诊。
【现病史及家族史】
患者1个月前无明显诱因出现上腹部不适、胀痛,无反酸、嗳气,无腹泻及黑便。母亲有“胃癌”病史。入院时生命体征平稳,巩膜无黄染,左锁骨上淋巴结未及,腹平软,未及明显包块,无明显压痛、反跳痛,移动性浊音(-),肠鸣音正常,**指诊未及异常。
【入院检查】
血常规无明显异常;血液生化检查未见明显异常;肿瘤标志物:癌胚抗原(CEA)69.28ng/ml.胃镜检查(2010年9月),提示贲门下胃体后壁见巨大溃疡,病变累及贲门口及胃底,大小约4×3cm,周边黏膜不规则(图1)。图1胃镜(2010年9月)贲门下胃体后壁见巨大溃疡,病变累及贲门口及胃底,大小约4×3cm,周边黏膜不规则病理检查为腺癌。CT检查(2010年9月),提示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影,考虑转移结节(图2)。



【病理检查】
为腺癌。CT检查(2010年9月),提示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影,考虑转移结节(图2)png]图2CT(2010年9月)示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影
【MDT讨论及诊治经过】
第一次MDT讨论(2010年10月)影像科该患者CT提示贲门下胃体小弯侧胃壁增厚,结合胃镜检查报告,胃癌诊断明确;CT示肝内多发低密度影,结合肿瘤标志物甲胎蛋白(AFP)不高,CEA考虑为转移结节,诊断为胃癌伴肝转移。肿瘤内科多数胃癌肝转移患者,全身化疗是主要治疗方法,但胃癌化疗目前尚无标准方案。常用化疗药5-氟尿嘧啶(5-Fu)及其前体药的口服剂(卡培他滨、替吉奥)、紫杉类(紫杉醇、多西他赛)、铂类(顺铂、奥沙利铂)。针对该患者可采用DCF3周方案。胃肠外科胃癌肝转移根据美国**综合癌症网络(NCCN)胃癌临床实践指南,主要采用化疗、纳入临床研究和最佳支持治疗等姑息措施。然而,也有一些研究表明对胃癌肝转移进行积极的综合治疗仍可使部分患者生存获益。治疗方案的选择应从以下方面考虑:①是同时性肝转移还是异时性肝转移;②评估肝脏转移灶大小、部位及多少,H1为转移灶局限于一个肝叶,H2为两个肝叶可见数个散在转移灶,H3为两个肝叶可见多量散在转移灶;③肝外有无转移灶;④原发病灶能否完全切除(R0)。对于原发灶能R0切除的H1型肝转移以及异时性肝转移应积极行一期联合切除或肝转移灶切除,而对于H2和H3型同时性肝转移,手术作为综合治疗手段之一可能有一定价值,但应慎重选择病例。肝脏外科对于胃癌肝转移的多个转移灶,建议行化疗、射频或介入等综合治疗,对孤立转移灶可考虑手术切除。针对该患者,建议化疗为主,手术为辅。消化内科对于中晚期胃癌,一般不考虑内镜下治疗。该患者无内镜下治疗的适应证。第一次治疗经过2010年10月采用DCF3周方案[多西他赛100mg/m2,第1天;顺铂20mg,1次/日,第1——5天;5-Fu750mg/m2,1次/日,第1——5天,每日持续静脉滴注6小时以上],解救化疗4个周期后,CT检查示胃壁肿块及肝转移灶均较前缩小,同前方案治疗共6个周期。2011年3月复查CEA48.26ng/ml,CT检查(图3)示贲门部胃壁增厚不明显,肝内未见明确低密度结节,复查胃镜示贲门下胃体后壁黏膜不规则隆起,2×2cm,累及贲门,临床评价部分缓解,改卡培他滨单药维持。图3CT(2011年3月)示贲门部胃壁增厚不明显,肝内未见明确低密度结节2011年9月CEA升高为91.20ng/ml,CT示肝脏转移灶增大(图4)。图4CT(2011年9月)示肝脏转移灶再次出现2011年9月再次组织全院胃癌MDT讨论。


【第二次MDT】
讨论(2011年9月)影像科2011年9月CT检查示贲门部胃壁增厚,肝脏内见数个圆形低密度影,大小分别为2.8×2.4cm、1.2×1.1cm、1.1×1.0cm,与周围组织分界欠清,结合第一次的CT,考虑肝多发转移,胃癌复发。肿瘤内科患者目前胃癌复发,在DCF方案效果不佳情况下,可考虑TCF(紫杉醇+顺铂+替加氟)等方案,也可考虑其他化疗方案,患者耐受性很差的情况下甚至可选择卡培他滨或替吉奥单药化疗。针对该患者建议行人表皮生长因子受体2(HER2)等相关检测,以决定是否需要考虑联合靶向药物治疗。胃肠外科胃癌肝转移手术治疗是一种姑息性治疗手段,在没有并发症前提下手术意义不大。针对该患者用改良DCF方案化疗6个周期,卡培他滨单药维持后,转移灶消失后复现,无梗阻、出血等并发症,无法R0切除,不建议手术。肝脏外科患者目前仍不具备肝脏转移灶R0切除条件,仍不建议手术。介入科该患者属于胃癌合并同时性肝脏多灶性转移,通过一线化疗方案,肝脏转移灶消失后复现,CEA升高。由于胃病灶与肝脏转移灶均存在,介入治疗无法完全根治。目前可参考肿瘤科的意见,更换二线化疗方案,当二线方案失效后,再考虑介入治疗。
【第二次治疗经过】
2011年9月采用TOF二线方案化疗(紫杉醇60mg/m2,第1、8天;奥沙利铂65mg/m2,第1、8天;5-Fu750mg/m2,1次/日,第1——5天,每日持续静脉滴注6小时以上,3周为一疗程,两个疗程后复查CT提示肝多发转移灶较前缩小,原最大病灶变为1.7×1.5cm.2012年1月继续维持此方案化疗4个周期后,患者耐受良好,改卡培他滨单药口服维持。2013年4月定期复查CT和CEA等肿瘤标志物,病情时有反复,交替更换化疗方案对症处理至今,目前一般状况尚可,时有上腹不适及乏力等症状,胃镜检查示贲门下胃体后壁见黏膜高低不平,大小约4×4cm(图5)。图5胃镜检查(2013年4月)示贲门下胃体后壁见黏膜高低不平,大小约4×4cm磁共振成像(MRI)检查示肝内多发转移结节较前增多增大(图6),CEA170.48ng/ml,行进一步治疗中。图6MRI(2013年4月)示肝内多发转移结节较前增多增大



【MDT治疗体会】
肝脏是胃癌远处转移最常见的靶器官。术前已明确或术中发现的肝转移占2.0%——9.9%.胃癌肝转移(GCLM)不仅预后差(5年生存率
既往史
【病例摘要】
【病史】
患者男性,65岁,因上腹部不适1个月于2010年9月来我院胃肠外科就诊。
【现病史及家族史】
患者1个月前无明显诱因出现上腹部不适、胀痛,无反酸、嗳气,无腹泻及黑便。母亲有“胃癌”病史。入院时生命体征平稳,巩膜无黄染,左锁骨上淋巴结未及,腹平软,未及明显包块,无明显压痛、反跳痛,移动性浊音(-),肠鸣音正常,**指诊未及异常。
【入院检查】
血常规无明显异常;血液生化检查未见明显异常;肿瘤标志物:癌胚抗原(CEA)69.28ng/ml.胃镜检查(2010年9月),提示贲门下胃体后壁见巨大溃疡,病变累及贲门口及胃底,大小约4×3cm,周边黏膜不规则(图1)。图1胃镜(2010年9月)贲门下胃体后壁见巨大溃疡,病变累及贲门口及胃底,大小约4×3cm,周边黏膜不规则病理检查为腺癌。CT检查(2010年9月),提示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影,考虑转移结节(图2)。



【病理检查】
为腺癌。CT检查(2010年9月),提示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影,考虑转移结节(图2)png]图2CT(2010年9月)示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影
【MDT讨论及诊治经过】
第一次MDT讨论(2010年10月)影像科该患者CT提示贲门下胃体小弯侧胃壁增厚,结合胃镜检查报告,胃癌诊断明确;CT示肝内多发低密度影,结合肿瘤标志物甲胎蛋白(AFP)不高,CEA考虑为转移结节,诊断为胃癌伴肝转移。肿瘤内科多数胃癌肝转移患者,全身化疗是主要治疗方法,但胃癌化疗目前尚无标准方案。常用化疗药5-氟尿嘧啶(5-Fu)及其前体药的口服剂(卡培他滨、替吉奥)、紫杉类(紫杉醇、多西他赛)、铂类(顺铂、奥沙利铂)。针对该患者可采用DCF3周方案。胃肠外科胃癌肝转移根据美国**综合癌症网络(NCCN)胃癌临床实践指南,主要采用化疗、纳入临床研究和最佳支持治疗等姑息措施。然而,也有一些研究表明对胃癌肝转移进行积极的综合治疗仍可使部分患者生存获益。治疗方案的选择应从以下方面考虑:①是同时性肝转移还是异时性肝转移;②评估肝脏转移灶大小、部位及多少,H1为转移灶局限于一个肝叶,H2为两个肝叶可见数个散在转移灶,H3为两个肝叶可见多量散在转移灶;③肝外有无转移灶;④原发病灶能否完全切除(R0)。对于原发灶能R0切除的H1型肝转移以及异时性肝转移应积极行一期联合切除或肝转移灶切除,而对于H2和H3型同时性肝转移,手术作为综合治疗手段之一可能有一定价值,但应慎重选择病例。肝脏外科对于胃癌肝转移的多个转移灶,建议行化疗、射频或介入等综合治疗,对孤立转移灶可考虑手术切除。针对该患者,建议化疗为主,手术为辅。消化内科对于中晚期胃癌,一般不考虑内镜下治疗。该患者无内镜下治疗的适应证。第一次治疗经过2010年10月采用DCF3周方案[多西他赛100mg/m2,第1天;顺铂20mg,1次/日,第1——5天;5-Fu750mg/m2,1次/日,第1——5天,每日持续静脉滴注6小时以上],解救化疗4个周期后,CT检查示胃壁肿块及肝转移灶均较前缩小,同前方案治疗共6个周期。2011年3月复查CEA48.26ng/ml,CT检查(图3)示贲门部胃壁增厚不明显,肝内未见明确低密度结节,复查胃镜示贲门下胃体后壁黏膜不规则隆起,2×2cm,累及贲门,临床评价部分缓解,改卡培他滨单药维持。图3CT(2011年3月)示贲门部胃壁增厚不明显,肝内未见明确低密度结节2011年9月CEA升高为91.20ng/ml,CT示肝脏转移灶增大(图4)。图4CT(2011年9月)示肝脏转移灶再次出现2011年9月再次组织全院胃癌MDT讨论。


【第二次MDT】
讨论(2011年9月)影像科2011年9月CT检查示贲门部胃壁增厚,肝脏内见数个圆形低密度影,大小分别为2.8×2.4cm、1.2×1.1cm、1.1×1.0cm,与周围组织分界欠清,结合第一次的CT,考虑肝多发转移,胃癌复发。肿瘤内科患者目前胃癌复发,在DCF方案效果不佳情况下,可考虑TCF(紫杉醇+顺铂+替加氟)等方案,也可考虑其他化疗方案,患者耐受性很差的情况下甚至可选择卡培他滨或替吉奥单药化疗。针对该患者建议行人表皮生长因子受体2(HER2)等相关检测,以决定是否需要考虑联合靶向药物治疗。胃肠外科胃癌肝转移手术治疗是一种姑息性治疗手段,在没有并发症前提下手术意义不大。针对该患者用改良DCF方案化疗6个周期,卡培他滨单药维持后,转移灶消失后复现,无梗阻、出血等并发症,无法R0切除,不建议手术。肝脏外科患者目前仍不具备肝脏转移灶R0切除条件,仍不建议手术。介入科该患者属于胃癌合并同时性肝脏多灶性转移,通过一线化疗方案,肝脏转移灶消失后复现,CEA升高。由于胃病灶与肝脏转移灶均存在,介入治疗无法完全根治。目前可参考肿瘤科的意见,更换二线化疗方案,当二线方案失效后,再考虑介入治疗。
【第二次治疗经过】
2011年9月采用TOF二线方案化疗(紫杉醇60mg/m2,第1、8天;奥沙利铂65mg/m2,第1、8天;5-Fu750mg/m2,1次/日,第1——5天,每日持续静脉滴注6小时以上,3周为一疗程,两个疗程后复查CT提示肝多发转移灶较前缩小,原最大病灶变为1.7×1.5cm.2012年1月继续维持此方案化疗4个周期后,患者耐受良好,改卡培他滨单药口服维持。2013年4月定期复查CT和CEA等肿瘤标志物,病情时有反复,交替更换化疗方案对症处理至今,目前一般状况尚可,时有上腹不适及乏力等症状,胃镜检查示贲门下胃体后壁见黏膜高低不平,大小约4×4cm(图5)。图5胃镜检查(2013年4月)示贲门下胃体后壁见黏膜高低不平,大小约4×4cm磁共振成像(MRI)检查示肝内多发转移结节较前增多增大(图6),CEA170.48ng/ml,行进一步治疗中。图6MRI(2013年4月)示肝内多发转移结节较前增多增大



【MDT治疗体会】
肝脏是胃癌远处转移最常见的靶器官。术前已明确或术中发现的肝转移占2.0%——9.9%.胃癌肝转移(GCLM)不仅预后差(5年生存率
个人史
【病例摘要】
【病史】
患者男性,65岁,因上腹部不适1个月于2010年9月来我院胃肠外科就诊。
【现病史及家族史】
患者1个月前无明显诱因出现上腹部不适、胀痛,无反酸、嗳气,无腹泻及黑便。母亲有“胃癌”病史。入院时生命体征平稳,巩膜无黄染,左锁骨上淋巴结未及,腹平软,未及明显包块,无明显压痛、反跳痛,移动性浊音(-),肠鸣音正常,**指诊未及异常。
【入院检查】
血常规无明显异常;血液生化检查未见明显异常;肿瘤标志物:癌胚抗原(CEA)69.28ng/ml.胃镜检查(2010年9月),提示贲门下胃体后壁见巨大溃疡,病变累及贲门口及胃底,大小约4×3cm,周边黏膜不规则(图1)。图1胃镜(2010年9月)贲门下胃体后壁见巨大溃疡,病变累及贲门口及胃底,大小约4×3cm,周边黏膜不规则病理检查为腺癌。CT检查(2010年9月),提示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影,考虑转移结节(图2)。



【病理检查】
为腺癌。CT检查(2010年9月),提示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影,考虑转移结节(图2)png]图2CT(2010年9月)示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影
【MDT讨论及诊治经过】
第一次MDT讨论(2010年10月)影像科该患者CT提示贲门下胃体小弯侧胃壁增厚,结合胃镜检查报告,胃癌诊断明确;CT示肝内多发低密度影,结合肿瘤标志物甲胎蛋白(AFP)不高,CEA考虑为转移结节,诊断为胃癌伴肝转移。肿瘤内科多数胃癌肝转移患者,全身化疗是主要治疗方法,但胃癌化疗目前尚无标准方案。常用化疗药5-氟尿嘧啶(5-Fu)及其前体药的口服剂(卡培他滨、替吉奥)、紫杉类(紫杉醇、多西他赛)、铂类(顺铂、奥沙利铂)。针对该患者可采用DCF3周方案。胃肠外科胃癌肝转移根据美国**综合癌症网络(NCCN)胃癌临床实践指南,主要采用化疗、纳入临床研究和最佳支持治疗等姑息措施。然而,也有一些研究表明对胃癌肝转移进行积极的综合治疗仍可使部分患者生存获益。治疗方案的选择应从以下方面考虑:①是同时性肝转移还是异时性肝转移;②评估肝脏转移灶大小、部位及多少,H1为转移灶局限于一个肝叶,H2为两个肝叶可见数个散在转移灶,H3为两个肝叶可见多量散在转移灶;③肝外有无转移灶;④原发病灶能否完全切除(R0)。对于原发灶能R0切除的H1型肝转移以及异时性肝转移应积极行一期联合切除或肝转移灶切除,而对于H2和H3型同时性肝转移,手术作为综合治疗手段之一可能有一定价值,但应慎重选择病例。肝脏外科对于胃癌肝转移的多个转移灶,建议行化疗、射频或介入等综合治疗,对孤立转移灶可考虑手术切除。针对该患者,建议化疗为主,手术为辅。消化内科对于中晚期胃癌,一般不考虑内镜下治疗。该患者无内镜下治疗的适应证。第一次治疗经过2010年10月采用DCF3周方案[多西他赛100mg/m2,第1天;顺铂20mg,1次/日,第1——5天;5-Fu750mg/m2,1次/日,第1——5天,每日持续静脉滴注6小时以上],解救化疗4个周期后,CT检查示胃壁肿块及肝转移灶均较前缩小,同前方案治疗共6个周期。2011年3月复查CEA48.26ng/ml,CT检查(图3)示贲门部胃壁增厚不明显,肝内未见明确低密度结节,复查胃镜示贲门下胃体后壁黏膜不规则隆起,2×2cm,累及贲门,临床评价部分缓解,改卡培他滨单药维持。图3CT(2011年3月)示贲门部胃壁增厚不明显,肝内未见明确低密度结节2011年9月CEA升高为91.20ng/ml,CT示肝脏转移灶增大(图4)。图4CT(2011年9月)示肝脏转移灶再次出现2011年9月再次组织全院胃癌MDT讨论。


【第二次MDT】
讨论(2011年9月)影像科2011年9月CT检查示贲门部胃壁增厚,肝脏内见数个圆形低密度影,大小分别为2.8×2.4cm、1.2×1.1cm、1.1×1.0cm,与周围组织分界欠清,结合第一次的CT,考虑肝多发转移,胃癌复发。肿瘤内科患者目前胃癌复发,在DCF方案效果不佳情况下,可考虑TCF(紫杉醇+顺铂+替加氟)等方案,也可考虑其他化疗方案,患者耐受性很差的情况下甚至可选择卡培他滨或替吉奥单药化疗。针对该患者建议行人表皮生长因子受体2(HER2)等相关检测,以决定是否需要考虑联合靶向药物治疗。胃肠外科胃癌肝转移手术治疗是一种姑息性治疗手段,在没有并发症前提下手术意义不大。针对该患者用改良DCF方案化疗6个周期,卡培他滨单药维持后,转移灶消失后复现,无梗阻、出血等并发症,无法R0切除,不建议手术。肝脏外科患者目前仍不具备肝脏转移灶R0切除条件,仍不建议手术。介入科该患者属于胃癌合并同时性肝脏多灶性转移,通过一线化疗方案,肝脏转移灶消失后复现,CEA升高。由于胃病灶与肝脏转移灶均存在,介入治疗无法完全根治。目前可参考肿瘤科的意见,更换二线化疗方案,当二线方案失效后,再考虑介入治疗。
【第二次治疗经过】
2011年9月采用TOF二线方案化疗(紫杉醇60mg/m2,第1、8天;奥沙利铂65mg/m2,第1、8天;5-Fu750mg/m2,1次/日,第1——5天,每日持续静脉滴注6小时以上,3周为一疗程,两个疗程后复查CT提示肝多发转移灶较前缩小,原最大病灶变为1.7×1.5cm.2012年1月继续维持此方案化疗4个周期后,患者耐受良好,改卡培他滨单药口服维持。2013年4月定期复查CT和CEA等肿瘤标志物,病情时有反复,交替更换化疗方案对症处理至今,目前一般状况尚可,时有上腹不适及乏力等症状,胃镜检查示贲门下胃体后壁见黏膜高低不平,大小约4×4cm(图5)。图5胃镜检查(2013年4月)示贲门下胃体后壁见黏膜高低不平,大小约4×4cm磁共振成像(MRI)检查示肝内多发转移结节较前增多增大(图6),CEA170.48ng/ml,行进一步治疗中。图6MRI(2013年4月)示肝内多发转移结节较前增多增大



【MDT治疗体会】
肝脏是胃癌远处转移最常见的靶器官。术前已明确或术中发现的肝转移占2.0%——9.9%.胃癌肝转移(GCLM)不仅预后差(5年生存率
查体
T:36.5℃,P:161次/分,R:12次/分,BP:135/80mmHg
【病例摘要】
【病史】
患者男性,65岁,因上腹部不适1个月于2010年9月来我院胃肠外科就诊。
【现病史及家族史】
患者1个月前无明显诱因出现上腹部不适、胀痛,无反酸、嗳气,无腹泻及黑便。母亲有“胃癌”病史。入院时生命体征平稳,巩膜无黄染,左锁骨上淋巴结未及,腹平软,未及明显包块,无明显压痛、反跳痛,移动性浊音(-),肠鸣音正常,**指诊未及异常。
【入院检查】
血常规无明显异常;血液生化检查未见明显异常;肿瘤标志物:癌胚抗原(CEA)69.28ng/ml.胃镜检查(2010年9月),提示贲门下胃体后壁见巨大溃疡,病变累及贲门口及胃底,大小约4×3cm,周边黏膜不规则(图1)。图1胃镜(2010年9月)贲门下胃体后壁见巨大溃疡,病变累及贲门口及胃底,大小约4×3cm,周边黏膜不规则病理检查为腺癌。CT检查(2010年9月),提示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影,考虑转移结节(图2)。



【病理检查】
为腺癌。CT检查(2010年9月),提示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影,考虑转移结节(图2)png]图2CT(2010年9月)示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影
【MDT讨论及诊治经过】
第一次MDT讨论(2010年10月)影像科该患者CT提示贲门下胃体小弯侧胃壁增厚,结合胃镜检查报告,胃癌诊断明确;CT示肝内多发低密度影,结合肿瘤标志物甲胎蛋白(AFP)不高,CEA考虑为转移结节,诊断为胃癌伴肝转移。肿瘤内科多数胃癌肝转移患者,全身化疗是主要治疗方法,但胃癌化疗目前尚无标准方案。常用化疗药5-氟尿嘧啶(5-Fu)及其前体药的口服剂(卡培他滨、替吉奥)、紫杉类(紫杉醇、多西他赛)、铂类(顺铂、奥沙利铂)。针对该患者可采用DCF3周方案。胃肠外科胃癌肝转移根据美国**综合癌症网络(NCCN)胃癌临床实践指南,主要采用化疗、纳入临床研究和最佳支持治疗等姑息措施。然而,也有一些研究表明对胃癌肝转移进行积极的综合治疗仍可使部分患者生存获益。治疗方案的选择应从以下方面考虑:①是同时性肝转移还是异时性肝转移;②评估肝脏转移灶大小、部位及多少,H1为转移灶局限于一个肝叶,H2为两个肝叶可见数个散在转移灶,H3为两个肝叶可见多量散在转移灶;③肝外有无转移灶;④原发病灶能否完全切除(R0)。对于原发灶能R0切除的H1型肝转移以及异时性肝转移应积极行一期联合切除或肝转移灶切除,而对于H2和H3型同时性肝转移,手术作为综合治疗手段之一可能有一定价值,但应慎重选择病例。肝脏外科对于胃癌肝转移的多个转移灶,建议行化疗、射频或介入等综合治疗,对孤立转移灶可考虑手术切除。针对该患者,建议化疗为主,手术为辅。消化内科对于中晚期胃癌,一般不考虑内镜下治疗。该患者无内镜下治疗的适应证。第一次治疗经过2010年10月采用DCF3周方案[多西他赛100mg/m2,第1天;顺铂20mg,1次/日,第1——5天;5-Fu750mg/m2,1次/日,第1——5天,每日持续静脉滴注6小时以上],解救化疗4个周期后,CT检查示胃壁肿块及肝转移灶均较前缩小,同前方案治疗共6个周期。2011年3月复查CEA48.26ng/ml,CT检查(图3)示贲门部胃壁增厚不明显,肝内未见明确低密度结节,复查胃镜示贲门下胃体后壁黏膜不规则隆起,2×2cm,累及贲门,临床评价部分缓解,改卡培他滨单药维持。图3CT(2011年3月)示贲门部胃壁增厚不明显,肝内未见明确低密度结节2011年9月CEA升高为91.20ng/ml,CT示肝脏转移灶增大(图4)。图4CT(2011年9月)示肝脏转移灶再次出现2011年9月再次组织全院胃癌MDT讨论。


【第二次MDT】
讨论(2011年9月)影像科2011年9月CT检查示贲门部胃壁增厚,肝脏内见数个圆形低密度影,大小分别为2.8×2.4cm、1.2×1.1cm、1.1×1.0cm,与周围组织分界欠清,结合第一次的CT,考虑肝多发转移,胃癌复发。肿瘤内科患者目前胃癌复发,在DCF方案效果不佳情况下,可考虑TCF(紫杉醇+顺铂+替加氟)等方案,也可考虑其他化疗方案,患者耐受性很差的情况下甚至可选择卡培他滨或替吉奥单药化疗。针对该患者建议行人表皮生长因子受体2(HER2)等相关检测,以决定是否需要考虑联合靶向药物治疗。胃肠外科胃癌肝转移手术治疗是一种姑息性治疗手段,在没有并发症前提下手术意义不大。针对该患者用改良DCF方案化疗6个周期,卡培他滨单药维持后,转移灶消失后复现,无梗阻、出血等并发症,无法R0切除,不建议手术。肝脏外科患者目前仍不具备肝脏转移灶R0切除条件,仍不建议手术。介入科该患者属于胃癌合并同时性肝脏多灶性转移,通过一线化疗方案,肝脏转移灶消失后复现,CEA升高。由于胃病灶与肝脏转移灶均存在,介入治疗无法完全根治。目前可参考肿瘤科的意见,更换二线化疗方案,当二线方案失效后,再考虑介入治疗。
【第二次治疗经过】
2011年9月采用TOF二线方案化疗(紫杉醇60mg/m2,第1、8天;奥沙利铂65mg/m2,第1、8天;5-Fu750mg/m2,1次/日,第1——5天,每日持续静脉滴注6小时以上,3周为一疗程,两个疗程后复查CT提示肝多发转移灶较前缩小,原最大病灶变为1.7×1.5cm.2012年1月继续维持此方案化疗4个周期后,患者耐受良好,改卡培他滨单药口服维持。2013年4月定期复查CT和CEA等肿瘤标志物,病情时有反复,交替更换化疗方案对症处理至今,目前一般状况尚可,时有上腹不适及乏力等症状,胃镜检查示贲门下胃体后壁见黏膜高低不平,大小约4×4cm(图5)。图5胃镜检查(2013年4月)示贲门下胃体后壁见黏膜高低不平,大小约4×4cm磁共振成像(MRI)检查示肝内多发转移结节较前增多增大(图6),CEA170.48ng/ml,行进一步治疗中。图6MRI(2013年4月)示肝内多发转移结节较前增多增大



【MDT治疗体会】
肝脏是胃癌远处转移最常见的靶器官。术前已明确或术中发现的肝转移占2.0%——9.9%.胃癌肝转移(GCLM)不仅预后差(5年生存率
辅助检查
【病例摘要】
【病史】
患者男性,65岁,因上腹部不适1个月于2010年9月来我院胃肠外科就诊。
【现病史及家族史】
患者1个月前无明显诱因出现上腹部不适、胀痛,无反酸、嗳气,无腹泻及黑便。母亲有“胃癌”病史。入院时生命体征平稳,巩膜无黄染,左锁骨上淋巴结未及,腹平软,未及明显包块,无明显压痛、反跳痛,移动性浊音(-),肠鸣音正常,**指诊未及异常。
【入院检查】
血常规无明显异常;血液生化检查未见明显异常;肿瘤标志物:癌胚抗原(CEA)69.28ng/ml.胃镜检查(2010年9月),提示贲门下胃体后壁见巨大溃疡,病变累及贲门口及胃底,大小约4×3cm,周边黏膜不规则(图1)。图1胃镜(2010年9月)贲门下胃体后壁见巨大溃疡,病变累及贲门口及胃底,大小约4×3cm,周边黏膜不规则病理检查为腺癌。CT检查(2010年9月),提示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影,考虑转移结节(图2)。



【病理检查】
为腺癌。CT检查(2010年9月),提示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影,考虑转移结节(图2)png]图2CT(2010年9月)示贲门下胃体小弯侧胃壁增厚,肝内多发低密度影
【MDT讨论及诊治经过】
第一次MDT讨论(2010年10月)影像科该患者CT提示贲门下胃体小弯侧胃壁增厚,结合胃镜检查报告,胃癌诊断明确;CT示肝内多发低密度影,结合肿瘤标志物甲胎蛋白(AFP)不高,CEA考虑为转移结节,诊断为胃癌伴肝转移。肿瘤内科多数胃癌肝转移患者,全身化疗是主要治疗方法,但胃癌化疗目前尚无标准方案。常用化疗药5-氟尿嘧啶(5-Fu)及其前体药的口服剂(卡培他滨、替吉奥)、紫杉类(紫杉醇、多西他赛)、铂类(顺铂、奥沙利铂)。针对该患者可采用DCF3周方案。胃肠外科胃癌肝转移根据美国**综合癌症网络(NCCN)胃癌临床实践指南,主要采用化疗、纳入临床研究和最佳支持治疗等姑息措施。然而,也有一些研究表明对胃癌肝转移进行积极的综合治疗仍可使部分患者生存获益。治疗方案的选择应从以下方面考虑:①是同时性肝转移还是异时性肝转移;②评估肝脏转移灶大小、部位及多少,H1为转移灶局限于一个肝叶,H2为两个肝叶可见数个散在转移灶,H3为两个肝叶可见多量散在转移灶;③肝外有无转移灶;④原发病灶能否完全切除(R0)。对于原发灶能R0切除的H1型肝转移以及异时性肝转移应积极行一期联合切除或肝转移灶切除,而对于H2和H3型同时性肝转移,手术作为综合治疗手段之一可能有一定价值,但应慎重选择病例。肝脏外科对于胃癌肝转移的多个转移灶,建议行化疗、射频或介入等综合治疗,对孤立转移灶可考虑手术切除。针对该患者,建议化疗为主,手术为辅。消化内科对于中晚期胃癌,一般不考虑内镜下治疗。该患者无内镜下治疗的适应证。第一次治疗经过2010年10月采用DCF3周方案[多西他赛100mg/m2,第1天;顺铂20mg,1次/日,第1——5天;5-Fu750mg/m2,1次/日,第1——5天,每日持续静脉滴注6小时以上],解救化疗4个周期后,CT检查示胃壁肿块及肝转移灶均较前缩小,同前方案治疗共6个周期。2011年3月复查CEA48.26ng/ml,CT检查(图3)示贲门部胃壁增厚不明显,肝内未见明确低密度结节,复查胃镜示贲门下胃体后壁黏膜不规则隆起,2×2cm,累及贲门,临床评价部分缓解,改卡培他滨单药维持。图3CT(2011年3月)示贲门部胃壁增厚不明显,肝内未见明确低密度结节2011年9月CEA升高为91.20ng/ml,CT示肝脏转移灶增大(图4)。图4CT(2011年9月)示肝脏转移灶再次出现2011年9月再次组织全院胃癌MDT讨论。


【第二次MDT】
讨论(2011年9月)影像科2011年9月CT检查示贲门部胃壁增厚,肝脏内见数个圆形低密度影,大小分别为2.8×2.4cm、1.2×1.1cm、1.1×1.0cm,与周围组织分界欠清,结合第一次的CT,考虑肝多发转移,胃癌复发。肿瘤内科患者目前胃癌复发,在DCF方案效果不佳情况下,可考虑TCF(紫杉醇+顺铂+替加氟)等方案,也可考虑其他化疗方案,患者耐受性很差的情况下甚至可选择卡培他滨或替吉奥单药化疗。针对该患者建议行人表皮生长因子受体2(HER2)等相关检测,以决定是否需要考虑联合靶向药物治疗。胃肠外科胃癌肝转移手术治疗是一种姑息性治疗手段,在没有并发症前提下手术意义不大。针对该患者用改良DCF方案化疗6个周期,卡培他滨单药维持后,转移灶消失后复现,无梗阻、出血等并发症,无法R0切除,不建议手术。肝脏外科患者目前仍不具备肝脏转移灶R0切除条件,仍不建议手术。介入科该患者属于胃癌合并同时性肝脏多灶性转移,通过一线化疗方案,肝脏转移灶消失后复现,CEA升高。由于胃病灶与肝脏转移灶均存在,介入治疗无法完全根治。目前可参考肿瘤科的意见,更换二线化疗方案,当二线方案失效后,再考虑介入治疗。
【第二次治疗经过】
2011年9月采用TOF二线方案化疗(紫杉醇60mg/m2,第1、8天;奥沙利铂65mg/m2,第1、8天;5-Fu750mg/m2,1次/日,第1——5天,每日持续静脉滴注6小时以上,3周为一疗程,两个疗程后复查CT提示肝多发转移灶较前缩小,原最大病灶变为1.7×1.5cm.2012年1月继续维持此方案化疗4个周期后,患者耐受良好,改卡培他滨单药口服维持。2013年4月定期复查CT和CEA等肿瘤标志物,病情时有反复,交替更换化疗方案对症处理至今,目前一般状况尚可,时有上腹不适及乏力等症状,胃镜检查示贲门下胃体后壁见黏膜高低不平,大小约4×4cm(图5)。图5胃镜检查(2013年4月)示贲门下胃体后壁见黏膜高低不平,大小约4×4cm磁共振成像(MRI)检查示肝内多发转移结节较前增多增大(图6),CEA170.48ng/ml,行进一步治疗中。图6MRI(2013年4月)示肝内多发转移结节较前增多增大



【MDT治疗体会】
肝脏是胃癌远处转移最常见的靶器官。术前已明确或术中发现的肝转移占2.0%——9.9%.胃癌肝转移(GCLM)不仅预后差(5年生存率
























































全部评论
请问如果患者入院时有心衰+糖尿病酮症酸中毒并高渗状态,如何控制头1-2小时输液速度?
1.部分酮症酸中毒患者的首发症状是腹痛,而且很剧烈。有的可以出现腹肌紧张。很多急诊医生会误认为是急腹症。 2.确诊酮症酸中毒的方法:血糖高、尿出现酮体、血酮升高、及有明显的酸中毒深慢呼吸意识障碍表现。 3.抢救的关键步骤是快速开通静脉通道,快速低渗补液,结合胃肠道给水,可以口服的以口服为主,不能口服的,需要迅速下胃管进行鼻饲。再者,PH<7.0者,给予5%碳酸氢钠治疗。 4.胰岛素的运用问题:血糖高者,可以静脉快速给药,然后以4—6U/h(成人)给药。视血糖情况调整。开始时至少1个小时测一次血糖。 5.由于糖尿病患者低血糖耐受比较差,所以在血糖小于13时可以改用葡萄糖加胰岛素治疗。 6.电解质的调整。该患者高钾是由于高渗性脱水所致,一般通过快速补液稀释之后,血钾会下降,所以见尿之后,必须补钾。 复习了一次糖尿病酮症的诊治。
说的很详细,学习不少东西了。
好病历,学习~谢谢