【入院检查】
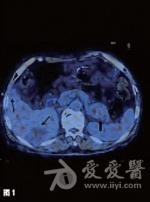
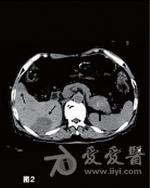
体检未见阳性体征,美国东部肿瘤协作组(ECOG)评分为1分。血常规、生化常规正常,空腹血清胃泌素(FSG)为1250pg/ml。上腹部磁共振成像(MRI)示胰尾部见一类圆形肿块,其大小为4cm×3cm,T1WI呈低、等信号,T2WI呈等、高信号,增强后见不均匀轻、中度强化;肝内可见多发的散在分布转移灶,大小为1.5cm×(1.5~5.4)cm×3.7cm。上消化道内镜检查示贲门溃疡,十二指肠降段至空肠上段多发溃疡;超声内镜检查示胰头、颈体部无明显异常回声,胰腺尾部见一稍低回声团,大小为2.85cm×3.87cm,境界尚清,推挤脾静脉,其旁未见明显肿大淋巴结回声。肝转移瘤穿刺活检病理:镜下见瘤细胞呈腺样排列,细胞大小较一致;免疫组化示胃泌素(Gas,+),突触素(Syn,+),CD56(+),CK20(+),CK19(+),CK7(+),癌胚抗原(CEA,-),CDX2(-),增殖细胞相关核抗原Ki67(1%,+),未找到核分裂,病变符合神经内分泌瘤。
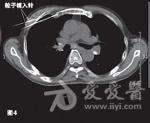
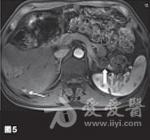
【胃泌素瘤治疗经过】
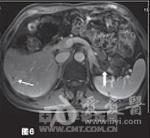
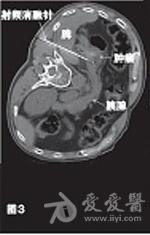
2008年10月患者于2008年10月至2011年11月共入院治疗12次,平均住院日为3天/次。明确诊断后即予奥美拉唑、奥曲肽、干扰素内科治疗。针对胰尾部肿瘤,先后行经皮经脾胰尾部肿物射频消融术(图3)和125I粒子植入术。针对肝脏转移瘤,共行3次肝动脉灌注化疗栓塞术(药物包括表柔比星、丝裂霉素、卡铂、5-氟尿嘧啶和碘化油),对较大转移病灶(5.4cm×3.7cm)联合射频消融治疗,影像学随访示肝内大部分病灶灭活。在整个治疗过程中,对胰尾部肿瘤和远处转移灶的治疗交替进行,并序贯联合应用上述各种微创治疗手段。2009年1月治疗开始3个月内,患者血清胃泌素水平降至正常,腹痛、腹泻等临床症状消失,胰腺病灶缩小,完全灭活,肝内转移瘤得到有效控制。2011年7月患者出现了胸骨转移,转移灶大小为1.2cm×1.0cm,行胸骨125I粒子植入术治疗(图4)。至今已随访该患者4年,其生理、免疫功能及生活质量基本未受影响。2012年8月MRI提示:胰尾部未见活性病灶,肝内病灶稳定(图5~6),胸骨转移灶活性消失。
【多学科团队讨论集绵】
影像介入科(诊断)胃泌素瘤患者上腹部MRI显示胰尾部肿块,T1WI见胰尾部低至中等信号的肿物,大小为4cm×3cm,增强后见病灶明显强化,信号稍高于胰腺正常部位。T1WI见肝内多发低、等信号,动脉期轻度强化,门脉期呈低信号,考虑为肝转移灶。另外,正电子发射体层摄影(PET)/CT也可见胰尾部软组织肿块代谢略活跃,肝脏数个低密度灶略活跃,考虑为胰腺恶性肿瘤伴肝内多发转移。胃胰外科结合胃泌素瘤患者病史,血清胃泌素水平,内镜、影像学检查及肝内肿物活检病理结果,可明确诊断为胰腺胃泌素瘤伴肝内多发转移。胃泌素瘤患者胰尾部肿瘤位置较深,其前方和外侧分别是胃和结肠脾曲,后方则是脾脏,行肿瘤外科切除时需先切除脾脏,这将对胃泌素瘤患者生理和免疫功能造成巨大的破坏。另外,影像学可见肝内多发转移灶,手术无法完全切除,故对该胃泌素瘤患者不推荐行手术治疗。内科目前认为,奥美拉唑、干扰素和生长抑素类似物(奥曲肽等)对晚期恶性胃泌素瘤,有一定的抑制肿瘤细胞生长的作用。因此,建议对该胃泌素瘤病例行奥美拉唑、奥曲肽和干扰素联合治疗,以减缓肿瘤细胞生长,缓解症状。影像介入科(临床)对于该胃泌素瘤患者,可首先采用肝动脉栓塞化疗联合射频消融,以清除肝内转移灶,减轻瘤负荷,再通过经皮经脾胰尾部肿物射频消融术联合放射性125I粒子植入术,灭活胰尾部原发肿瘤,这样就避免了外科创伤,也不必行脾脏的摘除。但在通过经皮经脾路径进行治疗时,应注意尽量避开邻近血管,精细操作,以避免脾破裂可能,防止大出血。一旦术中出现出血,应立即行脾脏栓塞止血治疗。
【病例分析】
鉴于目前的影像学检查很难发现较小的胰腺胃泌素瘤,结合患者主诉、病史,考虑其出现症状时已存在胰腺胃泌素瘤。患者入院时FS***平>1000pg/ml,腹部MRI示胰尾部肿物和肝内多发转移灶。原发灶最大径>2cm,超出胰腺组织,但未侵犯腹腔干和肠系膜上动脉;MRI示肝内多发转移,未见转移淋巴结,故根据第7版美国癌症联合委员会(AJCC)分期为Ⅳ期(cT3N0M1)。免疫组化示Gas(+),Syn(+),支持胃泌素瘤诊断,肝内多发转移说明恶性肿瘤,故诊断明确。
【肝转移的治疗】肝转移胃泌素瘤患者的5年生存率仅为17%~20%。目前国内外对胰腺胃泌素瘤肝转移尚无统一治疗方案。2010年美国**综合癌症网络(NCCN)指南建议,对肝转移瘤尽量行手术切除,而仅将肝脏区域性治疗(动脉栓塞、动脉化疗栓塞、动脉放射栓塞等)和局部消融治疗等微创方法作为姑息治疗手段之一。内科药物对胰腺胃泌素瘤,特别是已经发生转移的胃泌素瘤治疗作用非常有限,组胺、H2受体阻滞剂、质子泵抑制剂、奥曲肽、干扰素等可在一定程度上减缓肿瘤细胞生长,缓解症状,但无法缩小病灶、延长胃泌素瘤患者生存期。而目前研究认为,链佐星、多柔比星和5-氟尿嘧啶等化疗药物对原发灶和转移瘤也只有短期效果,无延长患者生存期的作用。
【胃泌素瘤治疗亮点】
肝转移是胰腺胃泌素瘤患者预后不良的主要因素,有20%~30%的患者在初诊时已存在肝转移。虽然肿瘤负荷是影响患者生存率的主要因素,但通过减瘤治疗,大部分患者仍可获得明显缓解,生存期延长。由于胃泌素瘤肝转移灶多呈多中心性,大部分病灶为多发、散在而无法完全切除,若原发灶局限且患者全身情况良好,传统认为可选择切除原发病灶加同种异体肝移植术治疗。但该方法阻止神经内分泌肿瘤向全身扩散的作用非常有限,且对人体生理和免疫功能造成巨大破坏,严重影响患者生活质量。该病例采用多学科团队综合治疗模式,在患者确诊后即行内科治疗,联合微创手段治疗胰腺原发灶和肝转移灶:针对胰腺病灶,采用经皮经脾胰尾部肿瘤射频消融术联合125I粒子植入,并在微创灭活胰尾部原发肿瘤的同时,序贯应用动脉栓塞化疗和局部消融术,使肝内大部分转移灶灭活,从而获得4年以上的疾病满意控制(胃泌素水平正常,症状消失,影像学检查见胰尾部肿瘤完全灭活,胸骨转移灶活性消失,肝内多发转移瘤大部分灭活)。
【微创治疗】
随着肿瘤医师和胃泌素瘤患者对生活质量的关注,个体化、人性化、理性化的建设性肿瘤治疗模式得到了更多的认可。影像学引导下的微创治疗由于定位精准,对正常组织创伤小,在有效灭活肿瘤的前提下,保护或改善了机体的生理、免疫功能,提高了胃泌素瘤患者的生活质量,在肿瘤的综合治疗中得到了广泛应用。对胰腺胃泌素瘤,通过包括微创治疗在内的MDT综合治疗,积极控制原发灶,可获得满意的疗效,改善胃泌素瘤患者的生活质量。因此,笔者认为微创介入治疗不仅是中晚期胰腺胃泌素瘤的主要治疗方法,也应该是早期胰腺胃泌素瘤的首选方法。
【微创多学科团队治疗模式】
10多年前,多学科团队率先提出包括影像引导下的微创或无创治疗的多学科团队综合治疗模式,在有效治疗肿瘤的前提下,最大限度地保护人体的生理和免疫功能,提高患者生活质量。该方法在本病例中的成功应用,开创了治疗胰尾部胃泌素瘤伴肝内多发转移的新模式。该模式也成功应用于原发性肝癌、胰腺癌、肺癌、乳腺癌等恶性实体瘤,获得了满意疗效。






全部评论